Evidenz und Studien
AQUACEL Ag+ Extra Wundverbände
![]()
Nachgewiesene Wirksamkeit
Die MEHR ALS SILBER™ Technologie in AQUACEL® Ag+ Extra™ Wundverbänden
- ermöglicht eine überlegene und anhaltende Anti-Biofilm Wirksamkeit gegen antibiotikaresistente Biofilme und verhindert ihren Wiederaufbau
- bietet gegenüber anderen silberhaltigen Wundverbänden eine höhere Anti-Biofilm Wirksamkeit
- fördert die Heilung bei stagnierenden chronischen Wunden
Unsere Studien & Untersuchungen belegen die Wirksamkeit!
Überlegene und anhaltende Anti-Biofilm Wirksamkeit und Verhinderung von Biofilm-Wiederaufbau
| Untersuchung | ||
| CA-MRSA in einem in vitro Biofilm Wundmodell.1 CA-MRSA (Community acquired MRSA) = ambulant erworbene Methicillinresistente Staphylococcus aureus. | ||
| Zielsetzung | ||
| Nachweis der antimikrobiellen Wirksamkeit von AQUACEL® Ag+ Extra™ und anderen silberhaltigen Wundverbänden gegen antibiotikaresistente Mikroorganismen in Bezug auf: • ihre Fähigkeit, Biofilm zu durchbrechen und die Mikroorganismen abzutöten. • ihre Fähigkeit, den Wiederaufbau von Biofilm (nach einer Wiederbeimpfung) zu verhindern. |
||
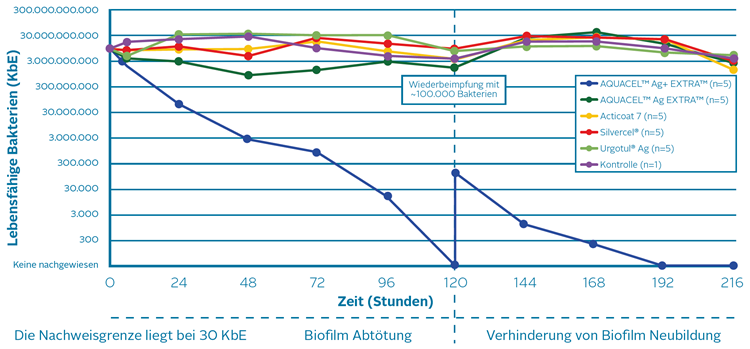 |
||
| Antimikrobielle Wirksamkeit von AQUACEL™ Ag+ Extra™, AQUACEL™ Ag Extra™, Acticoat 7, Silvercel® und Urgotul® Silver gegen CA-MRSA; Darstellung der Abtötung und Verhinderung von Biofilm-Wiederaufbau über 9 Tage. | ||
| Ergebnisse | ||
| AQUACEL® Ag+ Extra™ zeigte: | ||
| • schnellere Abtötung von CA-MRSA • Reduktion von Biofilm innerhalb von 6 Stunden nach Anlegen des Wundverbandes • Anhaltende Wirksamkeit nach der Wiederbeimpfung am 5. Tag |
||
Vergleich mit anderen silberhaltigen Wundverbänden
| Untersuchung | ||
| Echte Wundverhältnisse zu imitieren, ist eine Herausforderung. Basierend auf einem von UKAS* zertifiziertem CDC** Reaktormodell wurde ein in vitro Biofilm Modell mit gemischten Bakterienarten entwickelt. Der CDC Reaktor wurde für 72 Stunden unter Verwendung einer Suspension inkubiert, die Staphylococcus aureus, Pseudomonas aeruginosa und Candida albicans enthielt. Die Wundverbände wurden für 24 Stunden appliziert.2 | ||
| Zielsetzung | ||
| Der Vergleich der Anti-Biofilm Wirksamkeit von AQUACEL® Ag+ Extra™ mit einer Auswahl von gelbildenden Wundverbänden, die nur Silber enthalten. | ||
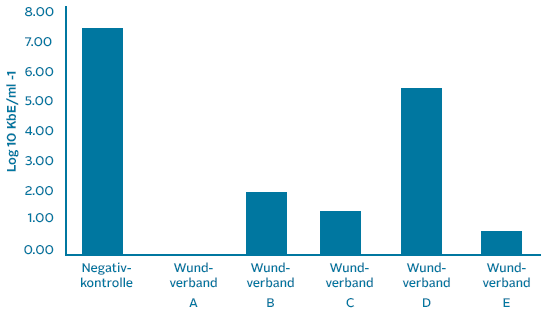 |
||
| Gesamtkeimzahl der lebensfähigen Bakterien nach 24-stündiger Behandlung eines über 72 Stunden gereiften Biofilms mit gemischten Bakterienarten. Wundverbände: A = AQUACEL™ Ag+ Extra™, B = UrgoClean™ Ag, C = Exufiber™ Ag+, D = Maxorb™ Extra Ag+, E = Kerracel™ Ag | ||
| Ergebnisse | ||
| Nur AQUACEL® Ag+ Extra™ reduzierte nach 24-stündiger Testdauer die lebensfähigen Mikroorganismen auf ein nicht mehr nachweisbares Niveau. | ||
Heilung bei stagnierenden chronischen Wunden
| Untersuchung | ||
| 111 Patienten mit stagnierenden und schwierigen Wunden aus 60 Kliniken in Großbritannien und Irland.3 | ||
| Zielsetzung | ||
| Nachweis der Fähigkeit von AQUACEL® Ag+ Extra™, Wundheilung bei chronischen Wunden zu fördern, die zu Beginn der Behandlung als stagnierend oder sich verschlechternd eingestuft wurden. | ||
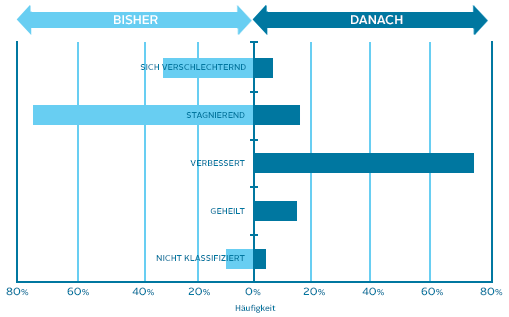 |
||
| Wundstatus zu Beginn der Behandlung mit AQUACEL® Ag+ Extra™ (Hellblau) und nach der Behandlung mit AQUACEL® Ag+ Extra™ (Dunkelblau). | ||
| Ergebnisse | ||
| • 78% der Wunden zeigten Heilungsfortschritte, 13% sind während des durchschnittlichen Bewertungszeitraums von 3,9 Wochen vollständig abgeheilt. • 83% der Wunden zeigten Heilungsfortschritte in den wesentlichen Wundheilungsparametern (Exsudat, Verdacht auf Biofiilm und Wundheilung). |
||
![]()
- WHRI5860 MA322-In Vitro Antimicrobial Activity of AQUACEL Ag + Extra and AQUACEL Ag Extra against Acticoat 7, Silvercel NA and Urgotul Ag -V1. Convatec Data on File. 27 November 2018.
- Assessment of the Anti-biofilm activity of silver-containing gelling fibre wound dressings, using a multi-species CDC reactor model. Hannah Thomas, Perfectus Biomed. Presented at Wounds UK November 2018. https://epostersonline.com/wounds2018/node/171 Accessed November 2018.
- Metcalf DG, Parsons D, Bowler PG. Clinical safety and effectiveness evaluation of a new antimicrobial wound dressing designed to manage exudate, infection and biofilm. Int Wound J 2017; 14: 203-213.